从源头优化阻断RAS限速步骤
肾素是RAS系统级联反应的限速步骤,其后的AngI、AngII乃至醛固酮的生成都直接或间接的受到肾素活性或其催化效率的调控。肾素将血管紧张素原转换为AngI的活性要远大于其他酶。因此,一旦阻断了肾素,便可在很大程度上阻断RAS。不同于传统的RAS抑制剂ACEI和ARB,阿利吉仑直接与肾素活性部位结合,从源头上阻断RAS,有效降低AngI、AngII和醛固酮水平(图1)。
唯一降低PRA的RAS抑制剂
PRA是每毫升血液中每小时生成AngI的量,是衡量RAS活性水平的指标,能够反映血浆中肾素催化血管紧张素原转化为AngI的能力,RAS激活以升高血压并介导非血压依赖性组织损伤,PRA与心血管事件发生率密切正相关,是心血管疾病的重要预测因子。研究结果表明,阿利吉仑可明显地降低PRA。为何DRI使PRA降低?这要从DRI阻断肾素活性的分子机制说起。肾素是一种蛋白水解酶,其分子由2个瓣叶组成、瓣叶间有一条裂隙,肾素的酶活性部位位于裂隙中。当血管紧张素原进入该裂隙,与肾素的酶活性部位发生接触后,血管紧张素原就被肾素水解、释放出AngI。如果DRI进入肾素分子的裂隙,占据了肾素的酶活性位点,肾素再也无法水解血管紧张素原。这种情况下,即使肾素分泌增多,PRA仍然降低。然而,ACEI和ARB 均使PRA升高(图1)。这是因为ACEI和ARB分别通过减少AngII的产生或阻断AngII的作用,削弱了AngII对肾素分泌的负反馈调节作用,导致肾素分泌增加和PRA升高。研究表明,DRI不但单药治疗降低PRA,与其他抗高血压药物联用时,还可中和后者引起的PRA升高,增强靶器官的保护效应,使得患者获得降压和降压以外的双重益处,这也为联合治疗提供了理论基础。阿利吉仑的问世无疑是高血压治疗领域的一大突破。
降压持久强效
阿利吉仑服用后1~3小时血药浓度达高峰,t1/2 大约为40小时,明显长于现有的ACEI和ARB,一天只需服用一次。因为其主要的排泄途径为原型从粪便中排出,所以与临床常用药物间相互作用少,肝肾功能损害的患者不用调整剂量。135L的表观分布容积使其可广泛地分布于血管外的组织,体内存留时间长。阿利吉仑的药代动力学特征决定了它的降压作用平稳而持久。临床研究也显示,阿利吉仑的降压疗效较现有降压药物相当或更优。阿利吉仑300mg的谷峰比长达0.98,且漏服一次后仍可保留超过91%的降压疗效,显著优于厄贝沙坦和雷米普利。
降低残余风险,最大优化临床获益
从RAS阻断效果来看,越来越多的研究发现,ACEI、ARB等对RAS的阻断并不理想,有关心血管死亡的坎地沙坦与安慰剂对比的CHARM-Overall试验结果显示:尽管接受坎地沙坦治疗,患者的心血管死亡率仍为18%。在雷米普利和安慰剂组对比的HOPE研究中,接受雷米普利治疗的患者主要心血管事件(心血管死亡、卒中和心肌梗死)的发生率为14%。可见,尽管ACEI/ARB治疗改善了患者的临床预后,但心血管风险和病死率,即残余风险仍然很高。其中的一个可能原因就是ACEI/ARB代偿性地升高PRA,不能理想的阻断RAS。有研究表明:与基线相比,阿利吉仑单药治疗有效降低PRA水平,联合治疗时能够抵消由其他抗高血压药物引起的PRA升高。阿利吉仑降低PRA的独特优点奠定了其在进一步降低残余心血管风险中的重要地位。
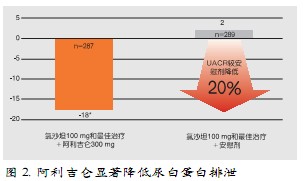
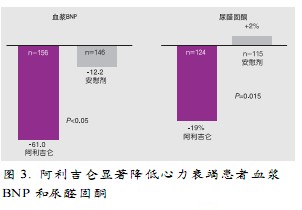
ASPIRE HIGHER临床研究计划中已完成的AVOID(Aliskiren in the Evaluation of Proteinuria in Diabetes)研究和ALOFT(Aliskiren Observation of Heart Failure Treatment)研究显示,在现有最佳治疗基础上加用阿利吉仑可进一步降低2型糖尿病肾病患者的尿蛋白(图2)和降低心力衰竭患者血浆B型尿钠肽和尿醛固酮水平(图3),且安全耐受。由此可见,阿利吉仑在器官保护方面发挥着积极作用,可最大化临床获益。
阿利吉仑的问世无疑为高血压治疗,特别是合并2型糖尿病肾病和心力衰竭的高血压患者提供了优化选择,它从源头上阻断RAS,降低PRA,降压强效持久,耐受性好。目前已有试验证实了其卓越的降压和靶器官保护的作用,正在进行的ASPIRE HIGHER研究将进一步夯实阿利吉仑降低残余风险,改善临床长期预后的作用。
quick 1 hour loans