编者按:对于一些器官功能衰竭的患者而言,移植是治疗的终极选择。虽然近年来器官移植的成功率不断提高,但器官供体短缺依旧是世界各国面临的难题。为此,医学家、材料学家、基因学家等各学科的研究者都在寻求除了人类自身以外的器官供体。目前,比较成熟的器官来源包括异种器官移植、3D生物打印器官、干细胞再生器官等,不一而足。第22届中国南方国际心血管病学术会议(SCC)上,中国人民解放军总医院第四医学中心姚斌医生分享了生物3D打印与器官再生最新研究进展。本刊特整理如下,以飨读者。
据不完全统计,全世界每年有将近200万人需要器官移植,但由于器官供体严重短缺,只有不到10%的患者可以等到器官并接受手术。目前世界范围内正在努力解决器官移植短缺的问题。
异种移植器官
异种移植器官是很有前景的应用方法,它能随时提供高质量、高生物安全性的细胞组织和器官。但是异种移植存在动物和人体跨种系的感染风险,即把人体和猪的细胞放在一起培养,人的细胞会感染猪的病毒,并且异种移植比同种移植存在更强的免疫排斥反应。
哈佛大学杨璐菡博士利用CRISPR-Cas9技术敲除了猪基因组中内源性逆转录病毒基因的所有拷贝,极大地推动了异种移植领域的研究进展。南京医科大学特聘教授戴一凡教授也在从事该领域的工作。
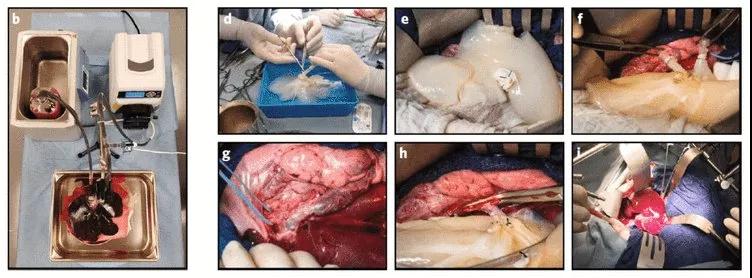
2021年6月24日,致力于使用猪器官进行人体异种移植的公司 Miromatrix Medical在纳斯达克上市,这是首个上市的异种器官移植公司。Miromatrix开发了其独有的灌注脱细胞和再细胞化(perfusion decellularization and recellularizatio)方法。他们使用泵洗细胞技术,将猪器官内的活细胞洗脱掉,只留下蛋白质框架,使结构和脉管系统完好无损。然后,再灌注人体细胞重新填充蛋白质框架,培养出可用于人体移植的器官。虽然这样免疫原性低,但是患者仍需要服用免疫抑制剂。
特定器官嵌合动物
近10年来,特定器官嵌合动物相关研究一直处于争议中。将一个物种的细胞注入另一物种的胚胎,会产生被称为“嵌合体”的动物。比如将动物受精卵某一个基因敲除,此时正常动物是无法出生的,将受精卵取出来,在囊胚期时注入人源iPS或者多能干细胞,这样有一定比例的动物细胞会发生胚胎补偿。比如敲除小鼠的胰腺发育基因,由于胚胎补偿机制,小鼠会生成一个由人的细胞构成的胰腺。嵌合效率、发育时间和供体细胞状态、进化关系有关。供体细胞指的是人体提供的多能干细胞,发育时间指获取干细胞的时间,进化关系即指亲源性,例如人和小鼠,人和猪的细胞可进行嵌合,但是小鼠和猪的亲缘关系太远,无法嵌合。
2017年美国索尔克研究所(Salk Institute)的科学家将人和猪的细胞进行嵌合,他们把眼睛、心脏和胰腺的基因敲除,这样猪的胚胎就会生成人细胞构成的眼睛、心脏和胰腺,但是为了评估这项技术的安全性和有效性,研究人员在第28天就终止了妊娠。理想状态下,注入的细胞倾向于向缺失的器官进行嵌合,但是也有可能嵌合到大脑里,因为人和动物的认知差别只在大脑皮层,人只有大脑皮层的神经元数量是显著多于其他物种的,如果注入的细胞有一定概率嵌合到猪的大脑皮层,这样猪的认知能力可能会很大程度上接近于人。此外,还有可能会嵌合到生殖系统,如精子、卵子,这些嵌合动物是不能相互繁殖的,否则它们体内的人的基因会不断纯化,造成伦理上的灾难性后果。
生物3D打印技术
3D打印就是将患者体内细胞提取出来,在体外和材料混合以后,打印出机械的支架,然后在体外培养成具有部分功能的器官,终极目标是构建具有完整功能的器官进行移植治疗。生物3D打印技术有喷墨式打印,激光辅助3D生物打印,挤出式生物打印和立体光刻成型。
三种器官再生技术比较
如表1所示,异体移植容易发生免疫排斥、病毒侵染,优点是来源丰富、成本低廉。嵌合体移植存在的问题则是编辑效率、血管(即嵌合器官是由人的细胞构成的,但血管和神经还是由宿主提供)、伦理限制,但来源丰富,无免疫排斥等问题。生物3D打印目前限制其发展的主要原因是缺少可用的生物材料和打印技术,可用于打印的、生物相容性好的,又能成型形成器官的材料很少,大部份材料硬度偏软,打印技术暂时也无法达到,倘若未来能够实现,生物3D打印可以快速量产且价格更低。
表1 三种器官再生技术比较

总而言之,异体移植和嵌合体更偏向于在动物体内发生,我们无法观察整个过程,只能通过结果去推断、修正,但是3D打印的整个过程是透明的,有问题可以随时更正,因此发展速度可能相对更快一些。 从学科角度来讲,分子生物学是自1953年沃森、克里克提出DNA分子的双螺旋结构模型才正式确立的,而生物材料、化学工程等已经发展多年,可能也是进展更快的原因,所以生物3D打印技术用于器官再生具有很好的应用前景。
优势与挑战
生物3D打印技术尚存在很多需要解决的问题,比如打印形成的器官细胞活性如何保证,血管化和神经化怎么去构建,水凝胶内细胞间的交流,细胞外基质的分泌,微环境的相互作用,器官功能的重建都是目前尚未解决的问题。目前3D生物打印的心脏只有一定的形态特征,缺乏异质性,不具有心脏的功能。
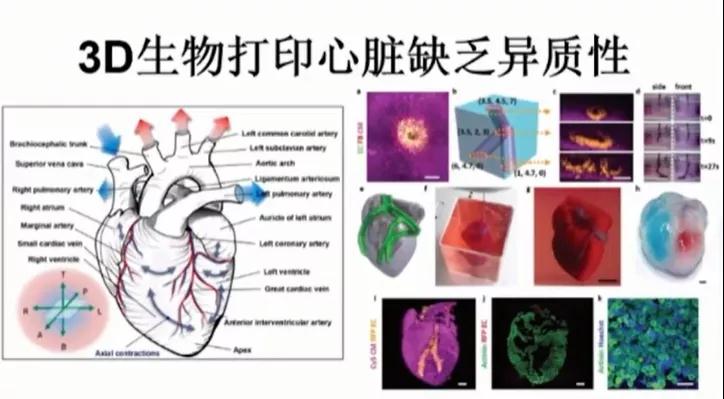
结构引导的器官再生与微组织工程
目前应用最多的是挤出式打印和立体光刻。挤出式打印可以用多个打印喷头构建细胞异质性,用不同的细胞和生物墨水同时去做不同的结构,但是达不到很高的细胞密度,而且挤压式打印是靠重力堆积的,打印出来后材料会坍塌,达不到精度要求。立体光刻是通过光成型法,精度可以达到5~10微米,但由于是光直接照到细胞池里面,所以无法构建细胞异质性,而且毒性也比较大(表2)。
表2 不同3D打印技术的优缺点

近几年我们开展的研究主要针对介于二者之间的细胞球的打印,即在体外先构建一个有一定细胞密度的细胞球,再去打印,就会有一个二次形态发生的过程。3D打印高密度细胞球构建心脏发育与病变模型是先做一个心脏细胞球体,之后用精细的打印头进行精细化的排列,形成各种形状的分布,这些分布的细胞球经过培养后会融合在一起。这样和体内的功能会更相近一些,如果用不同的细胞种类来做就可以具有细胞的异质性,如果加入的是病理性细胞,构建的就是病理模型,可以用于药物筛选和疗效验证。
此外我们还需关注结构的重要性,不同器官的结构不同,打印出的细胞球如果给它一个特定的器官结构,它会按照器官结构去发生,按照结构的引导去增殖、迁移、分化,和体内的分布相似,非常“智能”。
生物3D打印最终目的是器官再生,但目前还无法实现。目前做的较为成熟的技术是3D打印支架促进组织再生。我们团队近几年对生物3D打印微环境与组织再生进行了一定探索,通过生物3D打印基质微环境调控汗腺再生机制,诱导骨髓间充质干细胞(MSC)向汗腺分化,分化效率高,机制研究发现结构本身会影响基因表达,诱导出的汗腺细胞能直接参与受损汗腺的修复。
此外我们还研究了生物墨水改性对细胞生物学行为的影响,发现藻酸盐裂解酶掺入藻酸盐/明胶生物墨水可改善材料体外降解特性,同时酶促可降解藻酸盐/明胶生物墨水性能良好且促细胞增殖和粘附。酶促可降解藻酸盐/明胶生物墨水极大提升了生物3D打印的细胞性能,为挤压式打印法提供了更适合体外及体内研究的生物墨水。



 京公网安备 11010502033353号
京公网安备 11010502033353号